عناصر رادیواکتیو موادی هستند که هستههای ناپایدار دارند و با انتشار تابشهای یونیزهکننده مانند آلفا، بتا و گاما به عناصر پایدار تبدیل میشوند. این عناصر در طبیعت یافت میشوند و برخی از آنها مانند اورانیوم و پلوتونیوم کاربردهای گستردهای در تولید انرژی هستهای و صنعت پزشکی دارند. با توجه به اهمیت و خطرات احتمالی این مواد، استفاده از آنها نیازمند رعایت دقیق پروتکلهای ایمنی است. تولید انرژی هستهای، پزشکی هستهای و روشهای تشخیصی پیشرفته از جمله کاربردهای مهم این عناصر هستند که تأثیر بسزایی در علوم و فناوریهای مدرن دارند.

تاریخچه کشف مواد رادیواکتیو چیست؟
کشف مواد رادیواکتیو به اواخر قرن نوزدهم بازمیگردد، زمانی که هنری بکرل در سال ۱۸۹۶ متوجه شد که نمکهای اورانیوم بدون نیاز به نور، خودبهخود بر روی صفحات عکاسی اثر میگذارند. این کشف انقلابی راه را برای تحقیقات بیشتر هموار کرد، تا اینکه ماری و پیر کوری موفق شدند عناصر جدیدی مانند رادیوم و پولونیوم را شناسایی کنند. این دستاوردها نه تنها مبانی فیزیک هستهای را شکل دادند، بلکه تأثیر عمیقی بر پزشکی، صنعت و انرژی هستهای گذاشتند. امروزه، مواد رادیواکتیو در حوزههای مختلف علمی و صنعتی نقش کلیدی دارند و همچنان موضوع پژوهشهای پیشرفته هستند.
مطالب مرتبط: جدول تناوبی شیمی چیست؟

نمونه های مواد رادیو اکتیو طبیعی و مصنوعی کدام ها هستند؟
مواد رادیواکتیو به دو دسته طبیعی و مصنوعی تقسیم میشوند. مواد رادیواکتیو طبیعی، مانند اورانیوم-۲۳۸، توریم-۲۳۲ و رادیوم-۲۲۶، در پوسته زمین یافت میشوند و بهصورت طبیعی در فرآیندهای زمینشناسی و کیهانی شکل گرفتهاند. در مقابل، مواد رادیواکتیو مصنوعی در آزمایشگاهها و راکتورهای هستهای تولید میشوند، مانند پلوتونیوم-۲۳۹، سزیوم-۱۳۷ و تکنسیم-۹۹م که کاربردهای گستردهای در صنایع انرژی، پزشکی هستهای و تحقیقات علمی دارند. این عناصر به دلیل ویژگیهای پرتوزاییشان نقش مهمی در پیشرفت فناوریهای مدرن ایفا میکنند.

چه ذراتی از مواد رادیواکتیو منتشر می شود؟
مواد رادیواکتیو هنگام تجزیه، ذرات پرانرژی منتشر میکنند که شامل ذرات آلفا، بتا و گاما هستند. ذرات آلفا، که از دو پروتون و دو نوترون تشکیل شدهاند، قدرت یونیزهکنندگی بالایی دارند اما نفوذپذیری کمی دارند و با یک ورق کاغذ متوقف میشوند. در مقابل، ذرات بتا که الکترونها یا پوزیترونهای پرسرعت هستند، نفوذ بیشتری دارند و میتوانند از لایههای نازک فلز عبور کنند. اشعه گاما، که تابش الکترومغناطیسی بسیار پرانرژی است، از مواد چگال مانند سرب عبور میکند و برای محافظت در برابر آن، نیاز به سپرهای ضخیم است. این تابشها در پزشکی، صنعت و انرژی هستهای کاربردهای مهمی دارند و مدیریت ایمن آنها امری حیاتی است.

کاربرد مواد رادیو اکتیو چیست؟
مواد رادیواکتیو کاربردهای گستردهای در حوزههای مختلف علمی و صنعتی دارند. در پزشکی، از ایزوتوپهای رادیواکتیو مانند تکنسیم-۹۹م برای تصویربرداری پزشکی و تشخیص بیماریها استفاده میشود. در صنعت، از تابشهای رادیواکتیو برای بررسی کیفیت جوشکاری، تشخیص نشتهای لوله و اندازهگیری ضخامت مواد بهره میبرند. در حوزه انرژی، اورانیوم و پلوتونیوم بهعنوان سوخت اصلی نیروگاههای هستهای به کار میروند و نقش حیاتی در تولید برق پاک و پایدار دارند. همچنین، این مواد در تحقیقات علمی برای مطالعه فیزیک هستهای، زمینشناسی و کیهانشناسی به کار گرفته میشوند و موجب پیشرفتهای چشمگیری در این علوم شدهاند. استفاده کنترلشده و ایمن از این مواد به توسعه فناوریهای نوین کمک میکند.

زباله های مواد رادیواکتیو را چگونه از بین میبرند؟
مدیریت زبالههای رادیواکتیو یک فرآیند پیچیده و حساس است که برای جلوگیری از آسیبهای زیستمحیطی و انسانی انجام میشود. این زبالهها ابتدا دستهبندی شده و بر اساس سطح پرتوزایی، روشهای خاصی برای دفع آنها اتخاذ میشود. زبالههای کمخطر معمولاً در مخازن محافظ دفن میشوند، در حالی که زبالههای با پرتوزایی بالا نیاز به انبارسازی در محیطهای ایزوله، مانند گودالهای زمینشناسی عمیق دارند. همچنین، برخی روشهای پیشرفته مانند بازیافت مواد رادیواکتیو و تبدیل آنها به اشکال کمخطر در حال توسعه است. رعایت استانداردهای ایمنی و اجرای دقیق پروتکلهای دفع این زبالهها برای حفظ محیط زیست و سلامت انسانها امری ضروری محسوب میشود.

اثرات زیان بار مواد رادیو اکتیو چیست؟
مواد رادیواکتیو میتوانند اثرات زیانباری بر سلامت انسان و محیطزیست داشته باشند. قرار گرفتن طولانیمدت در معرض تابشهای یونیزهکننده مانند آلفا، بتا و گاما ممکن است باعث آسیب به سلولهای بدن، افزایش خطر ابتلا به سرطان، جهشهای ژنتیکی و مشکلات سیستم ایمنی شود. همچنین، آلودگی زیستمحیطی ناشی از زبالههای هستهای میتواند منابع آبی، خاک و هوا را تحت تأثیر قرار دهد و به اکوسیستم آسیب برساند. برای کاهش این خطرات، رعایت استانداردهای ایمنی، استفاده از تجهیزات حفاظتی و مدیریت صحیح مواد رادیواکتیو امری ضروری است. کنترل دقیق و دفع ایمن این مواد به حفظ سلامت عمومی و پایداری محیطزیست کمک میکند.
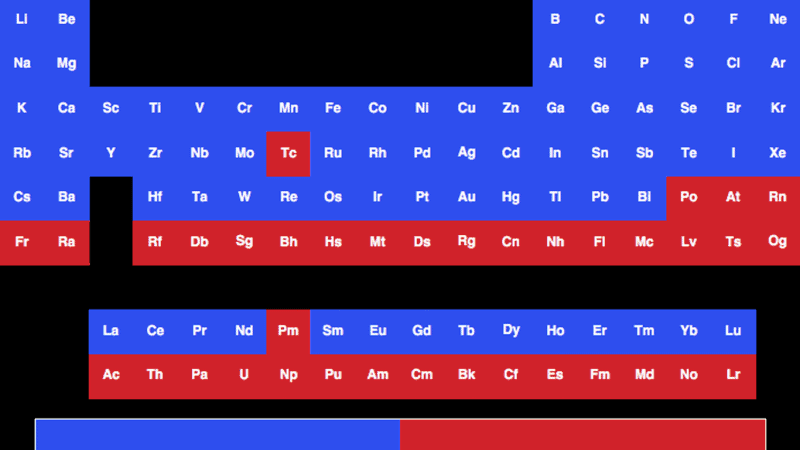
فهرست عناصر رادیو اکتیو در جدول تناوبی چیست؟
عناصر رادیواکتیو بسیاری وجود دارد که عدد اتمی و جرمی آنها، حالات فروپاشی و نیمه عمر آنها در جدول زیر آمده است.
| عنصر رادیواکتیو | عدد اتمی | عدد جرمی | نوع فروپاشی | نیمه عمر |
|---|---|---|---|---|
| هیدروژن | 1 | 3 | فروپاشی بتا (β-) | 32/12 سال |
| بریلیوم | 4 | 7 | گرفتن الکترون، فروپاشی گاما | 12/53 روز |
| بریلیوم | 4 | 8 | آلفا | 17- 10 × 7 ثانیه |
| بریلیوم | 4 | 10 | فروپاشی بتا (β-) | 1360000 سال |
| کربن | 6 | 14 | فروپاشی بتا (β-) | 5730 سال |
| کلسیم | 20 | 41 | گرفتن الکترون | 103000 سال |
| کلسیم | 20 | 46 | فروپاشی دوگانه بتا (β-β-) | 1015 × 8/2 سال |
| کلسیم | 20 | 48 | فروپاشی دو گانه بتا (β-β-) | 1019 × 4 |
| آهن | 26 | 54 | گرفتن الکترون مضاعف | 1022 × 1/3 سال |
| آهن سنتزی | 26 | 55 | گرفتن الکترون | 73/2 سال |
| آهن سنتزی | 26 | 59 | فروپاشی بتا (β-) | 503/44 روز |
| آهن سنتزی | 26 | 60 | فروپاشی بتا (β-) | 2600000 سال |
| کبالت سنتزی | 27 | 56 | گرفتن الکترون | 27/77 روز |
| کبالت سنتزی | 27 | 57 | گرفتن الکترون | 79/271 روز |
| کبالت سنتزی | 27 | 58 | گرفتن الکترون | 86/70 روز |
| کبالت سنتزی | 27 | 60 | فروپاشی بتا (β-)، گاما مضاعف | 2714/5 سال |
| نیکل | 28 | 59 | گرفتن الکترون | 76000 سال |
| نیکل سنتزی | 28 | 63 | فروپاشی بتا (β-) | 1/100 سال |
| روی سنتزی | 30 | 65 | گرفتن الکترون، گاما | 8/243 روز |
| روی سنتزی | 30 | 72 | فروپاشی بتا (β-) | 5/46 ساعت |
| سلنیوم | 34 | 79 | فروپاشی بتا (β-) | 105 × 27/3 سال |
| سلنیوم | 34 | 82 | فروپاشی بتا مضاعف (β- β-) | 1020 × 08/1 سال |
| کریپتون | 36 | 85 | فروپاشی بتا (β-) | 756/10 سال |
| روبیدیم | 37 | 87 | فروپاشی بتا (β-) | 1010 × 88/4 سال |
| استرونتیوم، | 38 | 89 | گرفتن الکترون، فروپاشی بتا (β-) | 52/50 روز |
| استرونتیوم، | 38 | 90 | فروپاشی بتا (β-) | 9/28 سال |
| ایتریم | 39 | 90 | فروپاشی بتا (β-)، گاما | 67/2 روز |
| ایتریم | 39 | 91 | فروپاشی بتا (β-)، گاما | 5/58 روز |
| زیرکونیم | 40 | 93 | فروپاشی بتا (β-) | 106 × 53/1 سال |
| زیرکونیم | 40 | 94 | فروپاشی بتا مضاعف (β-) | 1017 × 1/1 سال |
| زیرکونیم | 40 | 96 | فروپاشی بتا مضاعف (β-) | 1019 × 2 سال |
| نیوبیم | 41 | 93 | فروپاشی بتا (β-)، گاما | 13/16 سال |
| نیوبیم | 41 | 95 | فروپاشی بتا (β-)، گاما | 991/34 روز |
| مولیبدن | 42 | 93 | گرفتن الکترون | 103 × 4 سال |
| تکنتیوم | 43 | 99 | فروپاشی بتا (β-) | 105 × 111/2 سال |
| روتنیم | 44 | 103 | فروپاشی بتا (β-)، گاما | 26/39 روز |
| روتنیم | 44 | 106 | فروپاشی بتا (β-) | 59/373 روز |
| پالادیم | 46 | 107 | فروپاشی بتا (β-)، گاما | 5/6 میلیون سال |
| نقره | 47 | 111 | فروپاشی بتا (β-)، گاما | 45/7 روز |
| قلع | 50 | 126 | فروپاشی بتا (β-) | 105 × 3/2 سال |
| انتیمون | 51 | 125 | فروپاشی بتا (β-) | 7582/2 سال |
| تلوریم | 52 | 127 | فروپاشی بتا (β-)، گاما | 35/9 ساعت |
| تلوریم | 52 | 129 | فروپاشی بتا (β-) | 6/69 دقیقه |
| ید | 53 | 123 | گرفتن الکترون، گاما | 13 ساعت |
| ید | 53 | 129 | فروپاشی بتا (β-) | 7/15 میلیون سال |
| ید | 53 | 131 | گرفتن الکترون، گاما | 02070/8 روز |
| زنون | 54 | 125 | فروپاشی بتا (β-) | 9/16 ساعت |
| زنون | 54 | 127 | فروپاشی بتا (β-)، گاما | 345/36 روز |
| زنون | 54 | 133 | فروپاشی بتا (β-) | 247/5 روز |
| سزیم | 55 | 134 | گرفتن الکترون، فروپاشی بتا (β-) | 0648/2 سال |
| سزیم | 55 | 135 | فروپاشی بتا (β-) | 3/2 میلیون سال |
| سزیم | 55 | 137 | فروپاشی بتا (β-)، گاما | 17/30 سال |
| سزیم | 58 | 144 | فروپاشی بتا (β-) | 258 روز |
| پرومتیم | 61 | 147 | فروپاشی بتا (β-)، گاما | 6234/2 سال |
| اروپیم | 63 | 154 | فروپاشی بتا (β-)، فروپاشی بتا (β+), | |
| گاما | 16 سال | |||
| اروپیم | 63 | 155 | فروپاشی بتا | 2 سال |
| ایریدیم سنتزی | 77 | 188 | گرفتن الکترون | 73/1 روز |
| ایریدیم سنتزی | 77 | 189 | گرفتن الکترون | 2/13 روز |
| ایریدیم سنتزی | 77 | 190 | گرفتن الکترون | 8/11 روز |
| ایریدیم سنتزی | 77 | 192 | فروپاشی بتا (β-) ، گرفتن الکترون | 827/73 روز |
| ایریدیم سنتزی | 77 | 192 | فروپاشی بتا (β-) | 241 سال |
| ایریدیم سنتزی | 77 | 193 | فروپاشی بتا (β-) | 5/10 روز |
| ایریدیم سنتزی | 77 | 194 | فروپاشی بتا (β-) | 3/19 ساعت |
| ایریدیم سنتزی | 77 | 194 | فروپاشی بتا (β-) | 171 روز |
| سرب | 82 | 210 | فروپاشی بتا (β-)، آلفا | 21 سال |
| بیسموت | 83 | 210 | آلفا | 3 میلیون سال |
| پولونیم | 84 | 210 | فروپاشی بتا (β-) | 138 روز |
| رادون | 86 | 220 | آلفا، فروپاشی بتا (β+) | 1 دقیقه |
| رادون | 86 | 222 | آلفا | 4 روز |
| رادیوم | 88 | 224 | آلفا | 4 روز |
| رادیوم | 88 | 225 | فروپاشی بتا (β-) | 15 روز |
| رادیوم | 88 | 226 | آلفا | 622/1 سال |
| توریم | 90 | 228 | آلفا | 2 سال |
| توریم | 90 | 229 | آلفا | 340/7 سال |
| توریم | 90 | 230 | آلفا | 80000 سال |
| توریم | 90 | 232 | آلفا | 14 سال |
| توریم | 90 | 234 | فروپاشی بتا (β-) | 24 روز |
| پروتاکتینیم | 91 | 234 | فروپاشی بتا (β-) | 75/6 ساعت |
| اورانیوم | 92 | 233 | آلفا | 200/159 سال |
| اورانیوم | 92 | 234 | آلفا | 245500 سال |
| اورانیوم | 92 | 235 | آلفا | 108 × 038/7 سال |
| اورانیوم | 92 | 236 | 107 × 342/2 سال | |
| اورانیوم | 92 | 238 | آلفا | 468/4 میلیارد سال |
| نپتونیم سنتزی | 93 | 237 | آلفا | 144/2 میلیون سال |
| پلوتونیوم | 94 | 238 | آلفا | 74/87 سال |
| پلوتونیوم | 94 | 239 | آلفا | 104 × 41/2 سال |
| پلوتونیوم | 94 | 240 | آلفا | 103 × 5/6 سال |
| پلوتونیوم | 94 | 241 | فروپاشی بتا (β-) | 14 سال |
| پلوتونیوم | 94 | 242 | آلفا | 105 × 73/3 سال |
| پلوتونیوم | 94 | 244 | آلفا | 107 × 08/8 سال |
| امریکیم | 95 | 241 | آلفا | 2/432 سال |
| امریکیم | 95 | 242 | آلفا، گاما | 141 سال |
| امریکیم | 95 | 243 | آلفا | 370/7 سال |
| کوریم | 96 | 242 | آلفا | 160 روز |
| کوریم | 96 | 243 | آلفا | 1/29 سال |
| کوریم | 96 | 244 | آلفا | 1/18 سال |
| کوریم | 96 | 247 | آلفا | 6/15 میلیون سال |
نتیجه گیری
عناصر رادیواکتیو نقش مهمی در علوم، صنعت و پزشکی دارند و تأثیرات گستردهای بر فناوریهای مدرن گذاشتهاند. از کاربرد آنها در تولید انرژی گرفته تا تشخیص بیماریهای پزشکی، این مواد تحولات بزرگی را ایجاد کردهاند. با این حال، مدیریت ایمن و کنترل دقیق آنها ضروری است تا خطرات ناشی از تابشهای رادیواکتیو به حداقل برسد و سلامت انسان و محیطزیست حفظ شود. با رعایت استانداردهای ایمنی و استفاده مسئولانه، میتوان از فواید این عناصر بهرهمند شد و همزمان اثرات زیانبار آنها را کاهش داد. آینده تحقیقات در این حوزه، به کشف راههای جدید برای افزایش ایمنی و بهرهبرداری پایدار از این مواد وابسته است.




ثبت ديدگاه