جدول تناوبی شیمی از موضوعات پایه رشته شیمی است که هر فرد علاقهمند به رشته شیمی باید آن را بشناسد و از آن در انجام فعالیتهای شیمیایی استفاده کند. به جدول تناوبی، قانون تناوبی عناصر نیز گفته میشود که نحوه شکلگیری و تکمیل عناصر موجود بر روی کره زمین را نشان میدهد. جدول تناوبی همچنین قانون دورهای عناصر را تعیین میکند. زمانی که این جدول ساخته شد، رقابت دانشمندان برای یافتن دیگر عناصر این جدول افزایش یافت تا بتواند قطعات این جورچین را تکمیل کنند و آن را کامل کنند.
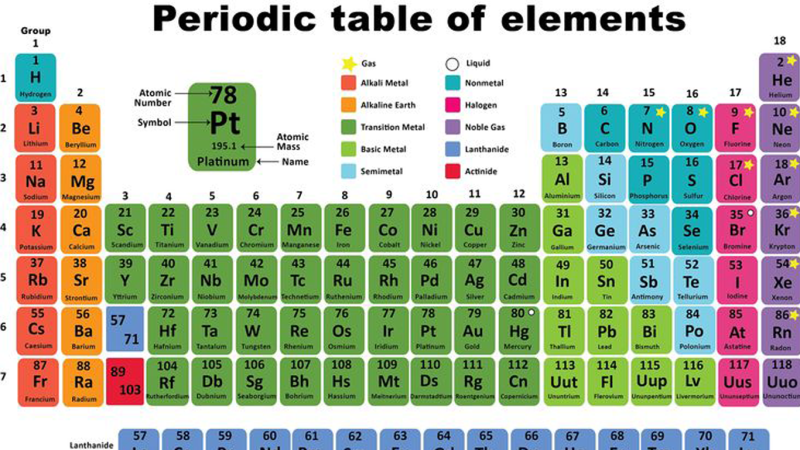
جدول تناوبی شیمی
تاریخچه جدول تناوبی
کشف کردن یک عنصر جدید اتفاقی مهم در علم شیمی و دنیای علم بوده است. کشف یک عنصر اعتبار بالایی برای کاشف آن به ارمغان میآورد. قبل از کشف جدول تناوبی، تعداد عناصر جدول تناوبی و خصوصیات آنها فقط به صورت حدس و گمان مطرح میشد. با کشف شدن جدول تناوبی عناصر، کشفی بزرگ در دنیای شیمی اتفاق افتاد که محدودیتهای بسیاری که شیمیدانان در آن زمان با آنها روبرو بودند را از بین برد. جدول تناوبی از موضوعات پایه و مهمی است که در علوم مختلف کاربرد دارد. میتوانید با مراجعه به محتوای کاربرد شیمی در پزشکی درباره گستردگی این علم زیبا بیاموزید.
در تاریخچه کشف جدول تناوبی حداقل 6 دانشمند از کشورهای مختلف و به صورت مستقل برای تکمیل و فرمولبندی آن کوشیدهاند. مندلیف از مشهورترین دانشمندانی است که برای ساخت جدول تناوبی تلاش کرده است. نظم و دستهبندی شگفتانگیز جدول تناوبی توسط مندلیف، ساختار و نظم را برای دنیای شیمی و شیمیدانان به ارمغان آورد. در این دستهبندی قالب ساختاری منسجمی برای عناصر در خانوادهها و گروههای مشخص وجود دارد که عناصر را در آنها دستهبندی کردهاند. همچنین مندلیف شجاعت کافی را داشت تا بتواند وجود داشتن و مشخصات عناصر کشف شده را مشخص و دستهبندی کند. همچنین او توانست مشخصات تعدادی از خانههای خالی جدول تناوبی را پیشبینی کند. 3 تا از عناصری که مندلیف توانست پیشبینی کند مربوط به عناصری بود که او آنها را ” اکا-بور”، “اکا-آلومینیوم” و “اکا-سیلیس” نامید. این 3 عنصر پس از 15 سال کشف شدند و به نامهای اسکاندیم، گالیم و ژرمانیم نامیده شدند.

جدول تناوبی شیمی
آنتوان لاووزیه از نخستین افراد در تعیین جدول تناوبی
آنتوان لاووزیه یک شیمیدان برجسته فرانسوی بود که شیمی نوین را بنیانگذاری کرد. او از نخستین افرادی بود که از ترازو برای اندازهگیری و تحقیق واکنشهای شیمیایی استفاده کرد. او از شخصیتهای برجسته در انقلاب شیمیایی در قرن 18 بود که نظریه تجربی را ارائه کرد. او همچنین واکنشهای شیمیایی اکسیژن و سیستم مدرن نامگذاری مواد شیمایی را بررسی کرد.
مطالب مرتبط: عناصر رادیواکتیو چیست؟
آنتوان لاووازیه یک محقق و آزمایشگر دقیق بود که دنیای شیمی را متحول کرد. او همچنین قانون پایستگی جرم را بنیان کرد و کشف کرد که واکنشهای تنفسی و احتراق در اثر واکنشهای شیمیایی با اکسیژن انجام میشود. یکی دیگر از دستاوردهای آنتوان لاووازیه، سیستم بندی نامگذاری شیمیایی است که به شیمیدانان بسیار کمک کرد. او قبل از انقلاب فرانسه از سرمایهداران برجستهای بود که در همین زمینه فعالیت میکرد، که در جریان ترور همراه با دیگر سرمایهداران اعدام شد.
جدول تناوبی شیمی
شاهکار مندلیف در تعیین جدول تناوبی
دیمیتری مندلیف از کسانی است که نقش برجستهای در توسعه علم شیمی داشته است. او با تنظیم جدول تناوبی و خواص و ویژگیهای هر عنصر توانست فعالیت شیمیدانان را سامان بخشد و موجب پیشرفت و نظم عناصر در علم شیمی شد. مندلیف هر عنصر و خواص مربوط به آنها را بر روی کارهایی نوشت و همه این کارتها را به دفعات متعدد براساس خصوصیات مختلف دسته بندی کرد. جدول تناوبی از اصول پایهای در شیمی است که کاربرد شیمی در زندگی را میتوانید ببینید.
پس از دستهبندی عناصر به روشهای مختلف، او به این نتیجه رسید که عناصر براساس افزایش جرم اتمی به گروههای مشخصی تقسیمبندی میشوند. در گروهبندی به این روش در هر ستون خصوصیات شیمیایی عنصرها یکسان است و در هر سطر عنصرها براساس افزایش جرم اتمی مرتب شدهاند. مندلیف قانون تناوبی عناصر را برای اولین بار در سال 1869 به انجمن شیمی-فیزیک پترزبورگ ارائه کرد. او پس از ارائه این قانون خود، به مدت 20 سال پس از آن بر روی شاهکار علمی خود کار کرد.

جدول تناوبی شیمی
علت شهرت جدول مندلیف چیست؟
شهرت این جدول بدلیل آن است که این جدول تمامی عناصری که تا آن زمان کشف نشده بودند را در خود جای داده است. دراین جدول گالیم اولین عنصری بود که در جدول مندلیف جای خالی داشت و او نام این عنصر را اکا-آلومینیوم یعنی شبه آلومینیوم گذاشته بود. این عنصر پس از کشف در جای خودش که به نام اکا-آلومینیوم خالی بود جایگزین شد. عناصر دیگری نیز مانند اسکاندیم و ژرمانیم جای آنها خالی بود و پس از کشف شدن در خانههای خالی قرار گرفتند. تنها عناصری که مندلیف حتی وجود داشتن آنها را پیشبینی نکرده بود، گازهای نجیب بودند. اما جالب است بدانید که این عناصر به شکلی کاملا منطقی پس از کشفشان جای خود را در جدول پیدا کردند.
برای مندلیف چیدن عناصر در یک گروه براساس خصوصیات شیمیایی یکسان به طبقهبندی آنها براساس افزایش جرم اتمی ارجحیت داشت. این دیدگاه مندلیف در دستهبندی عناصر در قرار گرفتن تلوریم و ید برخلاف جرم اتمیشان در جدول کاملا مشهود است.
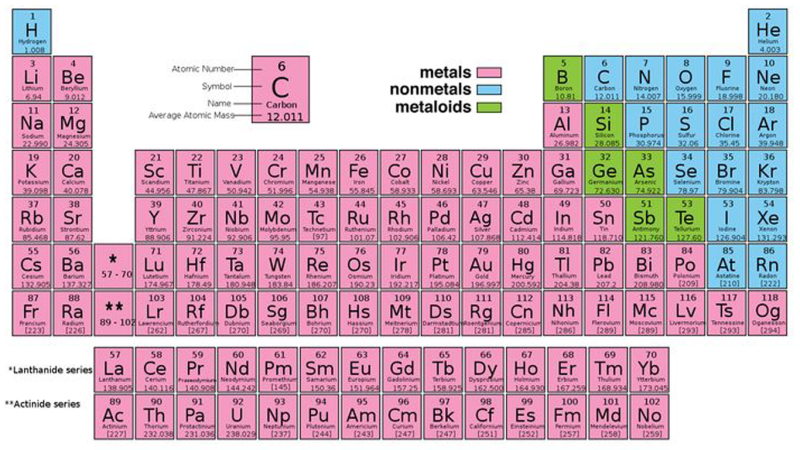
جدول تناوبی شیمی
جدول تناوبی عناصر شیمیایی
حدود 40 سال پس از کشف جدول تناوبی توسط مندلیف، این جدول باری دیگر دچار شوک جدیدی شد. این بار هنری موزلی با انجام آزمایشات بر روی پرتو ایکس توانست عدد اتمی عناصر را بدست بیاورد. موزلی کشف کرد که هر عنصر عدد اتمی مخصوص به خودش را دارد و به همین دلیل جدول مندلیف را به جای افزایش عدد جرمی برحسب افزایش عدد اتمی برای تمامی عناصری که کشف شده بودند، مرتب کرد.
در جدولی که موزلی ارائه داده بود نیز جای خالی برای عناصری که کشف نشده بودند، وجود داشت. ساختاری که موزلی برای جدول تناوبی ارائه داد بسیار به شکل امروزی آن نزدیک است. رشته شیمی دارویی از رشتههای پرکاربرد در صنایع است که در یادیگری ابتدایی آن نیاز به تسلط داشتن بر روی جدول تناوبی دارید.
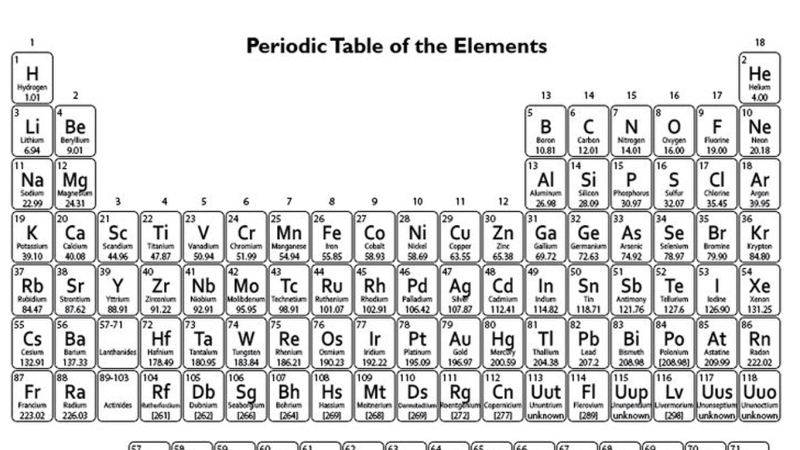
جدول تناوبی شیمی
گروه ها در جدول تناوبی عناصر شیمیایی
جدول تناوبی مندلیف دارای 18 ستون یا گروه است. در هر گروه از جدول تناوبی تعدادی عنصر قرار گرفته است که دارای خواص مشابهی هستند. این مدل طبقهبندی در گذشته انجام شده است، اما امروزه تنظیم گروههای جدول تناوبی براساس آرایش الکترونی انجام میشود که در لایه ظرفیت آنها وجود دارد. نامگذاری گروههای جدول تناوبی براساس سه روش استفاده از اعداد هندی، عربی و اعداد رومی انجام میشود. امروزه از اعداد رومی برای جدول تناوبی استفاده میشود. همچنین حروف انگلیسی A و B نیز برای عناصر گروههای اصلی و واسطه کاربرد دارد.

جدول تناوبی شیمی
ردیف در جدول تناوبی
در جدول تناوبی ردیفهایی به نام دوره یا تناوب وجود دارد که کمک میکند تا عناصری که دارای خواص شیمیایی یکسانی هستند در ستونهای زیر هم قرار بگیرند. در یک تناوب از جدول تناوبی هر عنصر نسبت به عنصر قبلی خود دارای یک پروتون و یک الکترون بیشتر دارد.

جدول تناوبی شیمی
گروه های شیمیایی در جدول تناوبی
گروه شیمیایی در جدول تناوبی نشاندهنده همان گروههای اصلی و واسطه جدول تناوبی هستند. هر کدام از گروههای شیمیایی در جدول نشاندهنده عناصری با تعداد الکترونهای یکسان در لایه ظرفیتشان هستند. به طور مثال عناصر گروه اول دارای یک الکترون، عناصر گروه دوم دارای دو الکترون در لایه ظرفیت خود هستند. به همین ترتیب تعداد الکترونهای لایه ظرفیت گروههای دیگر تعیین میشود.

جدول تناوبی شیمی
نتیجه گیری
جدول تناوبی عناصر توسط مندلیف برای اولین بار تنظیم شد، که انقلابی در علم شیمی محسوب میشد. در این جدول عناصر موجود برحسب عدد اتمی و شباهت خواص شیمیایی عناصر دستهبندی شدهاند.




ثبت ديدگاه