غلظت از موارد بسیار مهمی است که برای انجام آزمایشات شیمیایی و محاسبه فرمولها در مسائل شیمیایی نیاز به استفاده از آن داریم. غلظت برحسب مولاریته، مولالیته و … اندازهگیری میشود. همچنین از انواع واحدهای اندازهگیری ppm است که مفهوم آن به معنای قسمت در میلیون است و در مفهوم غلظت میتوان آن را معادل گرم حل شونده در یک میلیون گرم محلول یا میلی گرم حل شونده در 1000 گرم محلول دانست. اگر رقت محلول زیاد باشد میتوان فرض کرد که چگالی محلول همان چگالی حلال خالص است و اگر حلال را آب فرض کنیم میتوان گفت که ppm یعنی میلی گرم جسم حل شونده در یک لیتر محلول (یا یک لیتر آب).
با توجه به تعریف مولاریته (تعداد مول حل شونده در یک لیتر محلول) و مقایسه آن را با تعریف اخیر ppm
برای تبدیل کردن مولار به ppm باید تعداد مول حلشونده را برحسب میلی گرم حل شونده تبدیل کنیم. عدد به دست آمده همان غلظت محلول برحسب ppm است. برای یادگیری مولاریته روی لینک مولاریته چیست کلیک کنید.

تبدیل مولاریته به ppm
فرمول تبدیل مولاریته به ppm :
جرم مولی حل شونده* غلظت مولار*1000= غلظت ppm
مثال 1 :
محلول سدیم هیدروکسید 0.1 مولار با جرم مولی 40 گرم بر مول داریم. غلظت آن برحسب ppm چقدر است؟
تبدیل مولاریته به ppm
مثال 2 :
غلظت مولی محلول 200ppm پتاسیم نیترات با جرم مولی 101 گرم بر مول چند مولار است؟
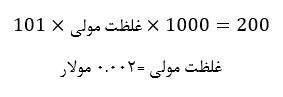
تبدیل مولاریته به ppm
مثال 3:
محلول 0.0003 مولار Cu+2 چند ppm است؟
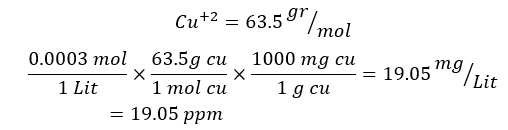
تبدیل مولاریته به ppm
مثال 4:
اگر محلول NaCl نسبت به یون کلر 3550ppm باشد غلظت مولار آن را را بدست بیاورید.
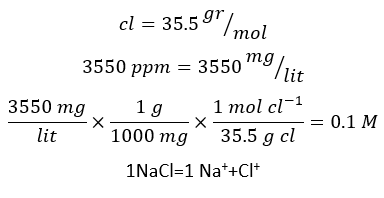
مثال 5 :
200 میلی لیتر از محلول Hcl با چگالی 1.2 گرم بر میلی لیتر و غلظت 0.001 مول بر لیتر موجود است. غلظت این محلول برحسب ppm تقریبا کدام است؟ (1mol HcL=36.5 g)
الف)30.4 ب)3.04 ج)40.4 د)4.04
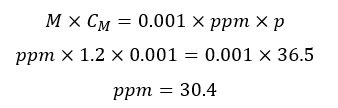
نتیجه گیری
غلظت ها از موارد بسیار مهم در شیمی و آزمایشگاههای شیمی هستند که شیمیدانان و افراد علاقهمند به شیمی باید آنها را فرا بگیرند. همچنین تبدیل انواع غلظتها به یکدیگر که در این مقاله آورده شده است از موارد بسیار مهم است.




ثبت ديدگاه